Lo que debes saber sobre la metodología por Quimioluminiscencia

Aplicación de Pruebas Rápidas en el Diagnóstico por COVID-19
febrero 16, 2021
¿Conoces la mejor opción para determinar Anticuerpos neutralizantes?
febrero 16, 2021Metodología por Quimioluminiscencia para determinar Anticuerpos IgG/IgM contra SARS CoV-2.
Test quimioluminiscente para determinar Anticuerpos contra COVID19
Se refiere a un inmunoensayo para la determinación de los anticuerpos IgG e IgM contra el nuevo coronavirus (SARS-CoV-2), en suero o plasma humano mediante un analizador para inmunoensayo de quimioluminiscencia completamente automatizado.
Los beneficios que pueden obtener con esta metodología quimioluminiscente son los siguientes:
- Determinación de anticuerpos IgG e Ig por separado, que permite diferenciar una infección por coronavirus en fase aguda de una pasada.
- Detección de anticuerpos con resultado numérico
- Ayudar a la detección temprana de casos sospechosos de SARS CoV-2 con prueba de ácido nucleico negativo
- Alto rendimiento para el montaje de alto volumen de pruebas.
- El kit de reactivos cuenta con controles propios.
- Configuración personalizada de muestras y reactivos
- La detección conjunta de Anticuerpos Anti SARS CoV-2 (IgG+IgM en kits separados) para garantizar una mejora de la sensibilidad clínica
- Confirmar en el paciente que ha estado en contacto con el virus, si ha generado inmunidad.
- Medir la cantidad de Anticuerpos generados contra el virus
- Resultado preciso de la prueba con solo 10 μL de volumen de muestra.
- Minimiza los riesgos de errores en al montaje de las muestras
- Permite hacer diluciones para muestras con alta concentración de Anticuerpos
- Utilidad adicional para identificar posibles donantes de plasma y evaluar la respuesta inmune post.vacunas.
Cuál es el fundamento de la prueba por Quimioluminiscencia?
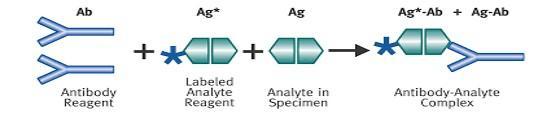
El ensayo de IgG del 2019-nCoV (CLIA) de MAGLUMI es un inmunoensayo de quimioluminiscencia indirecto.
Es un inmunoensayo de quimioluminiscencia indirecto, donde la muestra prediluida, el búfer y las microperlas magnéticas recubiertas con antígeno recombinante de 2019-nCoV se mezclan cuidadosamente y se incuban para formar inmunocomplejos. Después de la precipitación en un campo magnético, se decanta el sobrenadante y se realiza un ciclo de lavado. A continuación, se agrega aminobutiletilisoluminol (ABEI) marcado con anticuerpo IgG/IgM antihumano y se incuba para formar complejos. Después de la precipitación en un campo magnético, se decanta el sobrenadante y se realiza otro ciclo de lavado. Posteriormente, se agregan los iniciadores 1 + 2 para iniciar una reacción quimioluminiscente. La señal luminosa se mide con un fotomultiplicador como unidades de luz relativas (RLU), que es proporcional a la concentración del IgG/IgM de 2019-nCoV presente en la muestra.
¿Necesita esta prueba un equipo para realizar el procedimiento?
Los test por quimioluminiscencia, siempre necesitan de un analizador automatizado para obtener los resultados. En el procedimiento incluyen una calibración y montaje de controles para garantizar la calidad de los reportes. La automatización da la ventaja que no se realizan procedimientos manuales, las muestras son leídas por lector de código de barras y se pueden procesar muchas muestras en 1 solo montaje.
En que muestras se puede realizar el test?
La muestra ideal es suero o plasma, que se obtiene mediante la toma de muestra de sangre en tubo seco para obtener suero o con anticoagulante para obtener plasma, esta debe ser llevada a centrifugación y separarla de los glóbulos rojos.
Es importante centrifugar bien las muestras para que estén libres de fibrina y de hemólisis que pueden afectar los resultados.
En caso de conservar las muestras se deben guardar hasta por 3 días en temperatura de 2-8°C y por más tiempo en congelación a-20°C.
Qué características de rendimiento clínico deben tener las pruebas para la determinación de Anticuerpos IgG e IgM para SARS COV-2?
Según los lineamientos para el uso de pruebas diagnósticas de SARS-COV-2 (COVID- 19) en Colombia, deben cumplir con los siguientes requerimientos:
- Sensibilidad por encima del 85% y especificidad por encima del 90%
- Reporte sobre el porcentaje de correlación (tasa de coincidencia) con la PCR que es la prueba confirmatoria, debe ser mayor del 80%.
- Que el número de muestras con el cual la casa comercial hizo la validación sea como mínimo de 100.
¿Cuándo debe realizarse la prueba?
Las pruebas serológicas de anticuerpos IgM/IgG se indican para identificar el contacto previo de una persona con el virus SARS-CoV2. No se consideran pruebas diagnósticas y no se recomienda su uso para descartar un caso de infección aguda.
Según el Ministerio de salud se podrán realizar pruebas rápidas de anticuerpos IgM/IgG a las siguientes personas:
- Persona con síntomas leves sin factores de riesgo, se debe tomar la prueba nunca antes de 10 días de inicio de los síntomas.
- Contacto estrecho con síntomas leves y sin factores de riesgo, se debe tomar la prueba nunca antes de 10 días de inicio de los síntomas.
- Persona asintomática con o sin factores de riesgo que haya sido contacto estrecho de un caso confirmado
Sin embargo, su uso puede extenderse y aplicarse para tamizaje de población que potencialmente haya estado expuesta al virus en especial personal médico o paramédico para tomar medidas de aislamiento apropiadas.
Según los estudios recientes se ha observado que tras la infección se generan anticuerpos de tipo IgM y aunque parece que empiezan a elevarse aproximadamente 5-7 días tras la infección, los test los detectan mejor a los 8-14 días. Pasados 15-21 días aparecen los anticuerpos de tipo IgG.
¿Cómo es la interpretación de los resultados de la metodología por quimioluminiscente?
Los resultados obtenidos son numéricos y tienen un punto de corte para definir cuando el resultado es Reactivo y no Reactivo:
Mayor de 1.0 Au/mL se considera un resultado Reactivo (positivo)
Menor de 1.0 Au/mL se considera un resultado No Reactivo (Negativo)
En el caso de muestras con niveles de concentración cercanos al punto de corte o con resultados positivos se deben realizar pruebas de seguimiento. Si las pruebas de seguimiento no cambian significativamente, se deben complementar con resultados de prueba de PCR para aclarar el diagnóstico

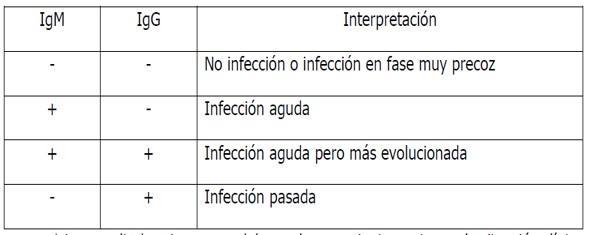
¿Cómo es la interpretación clínica de las pruebas serológicas?
Un resultado positivo indicaría infección por SARS-CoV-2 ya que implica la formación de inmunidad contra el virus.
Interpretación de pruebas serológicas combinadas con RT-PCR
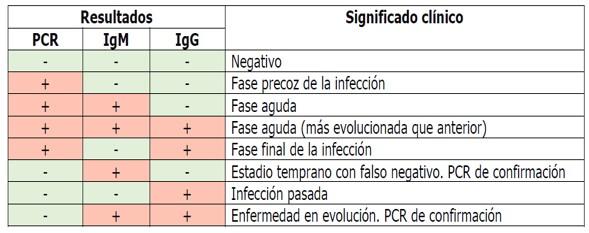
Tenga en cuenta que las pruebas serológicas de Anticuerpos IgG/igM por si solas no son pruebas diagnósticas, son complementarias con la prueba de PCR para llegar al diagnóstico confirmatorio de la infección por Covid 19.
Bibliografía
1. Lineamientos para el uso de pruebas diagnósticas de SARS-COV-2 (COVID- 19) en Colombia. https://www.minsalud.gov.co/RID/ lineamientos-pruebas-lsp-covid-19.pdf
2. Laboratory testing for 2019 novel coronavirus (2019-nCoV) in suspected human cases. Interim guidance. 19 March 2020. https:// www.who.int/publications-detail/laboratory-testing-for-2019-novel-coronavirus-in-suspected-human-cases-20200117. Consultado 31 marzo 2020.
3. Secretaría Distrital de Salud. Circular 041. Lineamiento de uso de pruebas serólogicas y emisión de resultado. Junio 5 de 2020. Bogotá.
4. Zhou, P., Yang, X., Wang, X. et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature (2020). https://doi.org/10.1038/s41586-020-2012-7.
5. Diagnosis and treatment program of novel coronavirus pneumonia (Trial version 7).
7. Na Zhu, Ph.D., Dingyu Zhang, et al.A Novel Coronavirus from Patients with Pneumonia in China, 2019[J].New England Journal of Medicine, 2020.
8. Prevention and control program of novel coronavirus pneumonia (version 5).