Diagnóstico serológico como opción no-invasiva en la detección de Helicobacter pylori

IMPORTANCIA DEL COLESTEROL HDL EN LA PREVENCIÓN DE ENFERMEDADES CORONARIAS
febrero 16, 2022
Importancia de la Medición de 25 OH Vitamina D
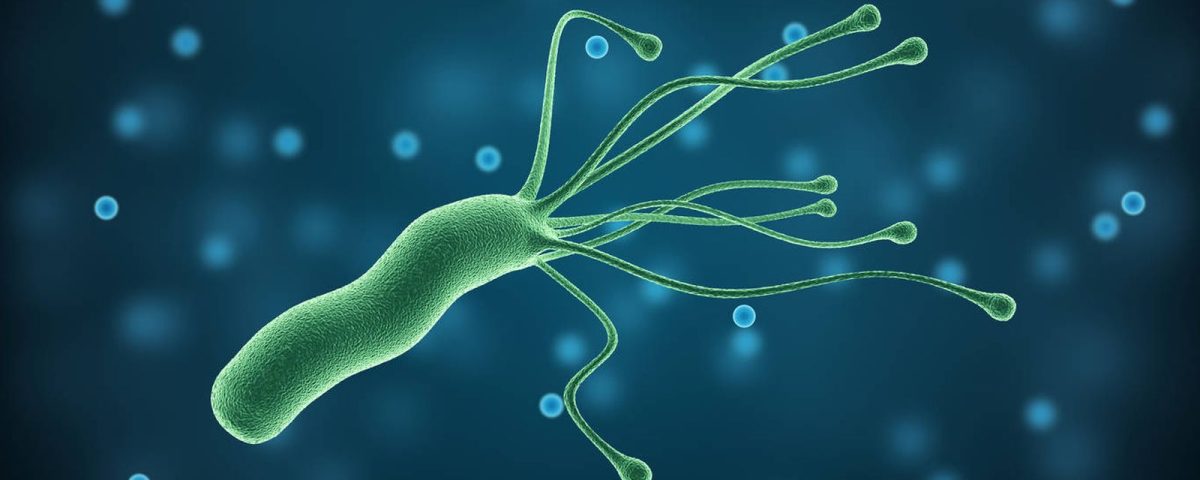
abril 19, 2022Helicobacter pylori es una bacteria gramnegativa que coloniza el estómago humano y se encuentra implicada en la patogenia de la dispepsia, úlcera péptica y cánceres gástricos. [1] Al colonizar el estómago de más del 50% de la población humana, con una mayor prevalencia en los países en vía de desarrollo que en los países desarrollados, se constituye en la infección crónica más frecuente en la especie humana [2].
Además del compromiso en el estómago, Helicobacter pylori se ha encontrado asociado con una gran variedad de enfermedades extradigestivas que afectan diferentes órganos o sistemas, entre las que se encuentran enfermedades de origen hematológico, dermatológico, reumatológico, cardiovascular, neurológico, oftalmológico y endocrinológico. Así como también con enfermedades pediátricas y gineco obstétricas, entre otras. Adicionalmente, en 1994, la Organización Mundial de la Salud reconoció la infección por Helicobacter pylori como un cancerígeno tipo I, el grado más alto de potencial carcinogénico, equiparándola, por ejemplo, con la asociación entre el hábito de fumar y el cáncer de pulmón; y, en 2003, esta misma Organización incluyó la infección por Helicobacter pylori en el ICD-10, reconociéndola como una enfermedad, similar a estar infectado por Treponema pallidum o por el virus de la inmunodeficiencia humana, que en todos los casos requiere intervención médica, identificación y erradicación.[3]
El diagnóstico de la infección por Helicobacter pylori se puede establecer por métodos invasivos, que dependen de la endoscopia digestiva alta que aparte de ser invasiva, costosa, molesta y no estar disponible en varias instituciones, no está exenta de complicaciones, algunas de extrema gravedad, y por métodos no-invasivos, los cuales no requieren endoscopia, como son la prueba de aliento con urea marcada con 13C, la detección de antígenos de Helicobacter pylori en materia fecal y la serología.
En el contexto del desarrollo tecnológico alrededor de Helicobacter pylori, la serología fue la primera prueba no-invasiva que se desarrolló para el diagnóstico de Helicobacter pylori, está disponible para uso clínico desde 1984, tan solo un año después de que la bacteria fuese cultivada a partir de muestras de mucosa gástrica tomadas de pacientes con gastritis. La prueba se basa en la identificación de anticuerpos específicos contra antígenos de Helicobacter pylori que aparecen como resultado de la respuesta inmunológica, tanto local como sistémica, en los individuos infectados [2] y suele mostrar un aumento transitorio de los anticuerpos IgM, seguido de un aumento de los anticuerpos IgG e IgA, que persiste durante la infección.[1]
El Consenso de Maastricht III y dispepsia, encargado de los lineamientos para manejo de la infección por H. pylori, ha rescatado la utilidad de la serología en el diagnóstico de la infección por este microorganismo en casos especiales, en particular cuando otras pruebas alternas pueden dar resultados falsos negativos, como sucede en pacientes con úlcera péptica sangrante, cuando se utiliza pruebas invasivas rápidas con ureasa (Clo-test), también cuando la carga de bacterias es muy baja para ser detectada (menor de 10.000 UFC/mL) y en los casos de gastritis atrófica, linfoma gástrico del MALT, cáncer gástrico, pacientes bajo terapia antibiótica o con inhibidores de la bomba de protones.[2] Por ello, cobra gran importancia contar con métodos serológicos de alta calidad analítica que eliminen las interferencias descritas anteriormente, de fácil procesamiento en plataformas automatizadas y económicos que puedan ofrecer alternativas diagnósticas valiosas.
Vélez Lab cuenta con las pruebas H. pylori IgA, IgG e IgM por la metodología de quimioluminiscencia (CLIA), en los analizadores MAGLUMI, que ayudan a aumentar la sensibilidad y especificidad en el diagnóstico de H. Pylori y monitorear el tratamiento y su erradicación ofreciendo una solución completa para cualquier tipo y tamaño de laboratorio clínico.
BIBLIOGRAFÍA
- P. Herbrink, L.J. van Doorn. Serological Methods for Diagnosis of Helicobacter pylori Infection and Monitoring of Eradication Therapy. Eur J Clin Microbiol Infect Dis 2000; 19 :164–173
- Campuzano-Maya G. Diagnóstico no-invasivo de Helicobacter pylori: ¿serología, prueba de aliento con 13C-urea o antígenos de Helicobacter pylori en materia fecal? Medicina & Laboratorio 2007; 13: 211-232.
- Campuzano-Maya G. Prueba de aliento optimizada con urea marcada con carbono 13 para la detección de Helicobacter pylori (PAU-Hp 13C). Medicina & Laboratorio 2012; 18: 3-4.